
Has the vaccination for Covid19 already been decided? who makes the vaccine and what does the vaccine consist of? mRNA vaccines, what exactly is an mRNA vaccine, what distinguishes it from an ordinary antibody vaccine? What is behind and what is behind mRNA?
Was ist das mRNA?
Als mRNA (englisch messenger RNA), auch Boten-RNA genannt, wird das einzelsträngige RNA-Transkript eines zu einem Gen gehörigen Teilabschnitts der DNA bezeichnet. Wird nun ein mRNA Impfstoff in den Körper eingebracht, so verändert sich die eigene DNA und somit der gesamte Körper.
Warum ist es sinnvoll dass mRNA kurzlebig ist?
Für Proteine, die im Bedarfsfall schnell „ausgeschaltet“ sein müssen, also nicht mehr vorhanden sein dürfen, ist deshalb eine kurzlebige mRNA von Vorteil. Dabei kann die Stabilität der mRNA durch Anhänge reguliert werden, die die RNA vor Abbau schützen. Fertig prozessierte mRNAs werden aus dem Kern geschleust! Was mit den abgebauten fertigen Prozessen im Körper geschieht ist nicht erforscht, bzw. bekannt. 60-70% der Tests an Tieren und Menschen waren fatal, die Tests endeten mit dem Kollabieren des Systems und dem Tod innerhalb weniger Stunden oder Tage.
Der Impfstoff Covid19 ist ein mRNA Impfstoff, welcher ca. 2-3 Monate getestet wurde und das jeweilige „Testobjekt“ binnen weniger Stunden des bitteren todes verstarb.
Bevor ein Impfstoff auf den Markt kommt, muss er ein umfassendes Zulassungsverfahren durchlaufen, entweder in Deutschland (nationale Zulassung durch das PEI) oder unter Mitwirkung des PEI bei der Europäischen Arzneimittelagentur EMA (zentrale europäische Zulassung durch die EU-Kommission). Zwingende Voraussetzung sind eine konsistente Herstellung, eine hohe Qualität und klinische Prüfungen in drei Phasen. Im Rahmen großer Zulassungsstudien der Phase III wird an mehreren tausend, manchmal mehreren zehntausend Teilnehmern nach deren informierten Zustimmung die Wirksamkeit und die Verträglichkeit/Sicherheit untersucht. Nur wenn der Nutzen eindeutig die Risiken überwiegt, wird ein neuer Impfstoff die Zulassung erhalten.
Link der Information Bundesgesundheitsministerium
Stellungnahme des Wissenschaftlichen Beirats des Paul-Ehrlich-Instituts, Bundesinstitut für Impfstoffe und biomedizinische Arzneimittel, zur Qualität und Sicherheit von Impfstoffen Impfen_Stellungnahme_Wiss_Beirat_PEI
„Die Entwicklung, Prüfung und Zulassung von Impfstoffen darf – auch auf europäischer und internationaler Ebene – angesichts einer Pandemie nicht beschleunigt werden“, fordert Mezis-Vorstandsmitglied Helmut Jäger.
Er betonte, das habe sich in der Vergangenheit mehrfach als Fehler erwiesen. Als Beispiel verwies er auf Impfstoffe, die bei der Schweinegrippe-Pandemie 2009 und bei der Dengue-Prävention 2017 auf den Philippinen eingesetzt worden seien.

Coalition for Epidemic Preparedness Innovations (CEPI)
Coalition for Epidemic Preparedness Innovations (CEPI) (engl. in etwa: Koalition für Innovationen in der Epidemievorbeugung), ist eine weltweite Allianz in öffentlich-privater Partnerschaft zwischen Regierungen, der WHO, der EU-Kommission, Forschungseinrichtungen, der Impfstoff-Industrie und privater Geldgeber, u. a. der Bill & Melinda Gates Foundation, zum Aufbau eines Forschungsnetzwerks zur Erforschung und Entwicklung neuer Impfstoffe zur besseren und direkteren Reaktion auf eventuell bevorstehende Ausbrüche neuer viraler Infekte.
Hintergrund
Die Ebolafieber-Epidemie 2014 hat die Weltgemeinschaft weitgehend unvorbereitet getroffen, und die Entwicklung von drei Impfstoffen kam zu spät und war nicht ausreichend.
Ebenso kam die Zikavirus-Epidemie 2015/2016 unvorbereitet und es gibt noch immer keinen Impfstoff dagegen. Diese Beispiele zeigten, dass wenig bekannte Viren plötzlich weltweite Epidemien auslösen können.
Diese Epidemien treten vor allem in Ländern mit geringer Versorgungs- und Forschungskapazität auf, Forschung und Industrie haben bei geringen Gewinnmargen wenig Interesse an einer Impfstoff-Entwicklung, außerdem bestehen bei länderübergreifenden Epidemien erhebliche legislative und administrative Probleme, um schnelle Gegenmaßnahmen starten zu können. Bei den bisherigen Epidemien neuer Viren zeigte sich zudem eine fragmentierte und stark unkoordinierte Aktivität der Regierungen, lokalen Public Health-Stellen und Forschungseinrichtungen. Aus der Einsicht, dass eine zügige Impfstoff-Entwicklung globale Epidemien abwenden kann, wurde die Forderung nach einem effizienten weltweiten System laut, das auf die Forschung und Entwicklung neuer Impfstoffe vorbereitet ist. Durch solche Plattformen soll die Entwicklungszeit verkürzt werden, sollen klinische Studien schneller lanciert werden und die Impfstoffherstellung beschleunigt werden.
Die WHO hat erstmals im Mai 2016 eine Liste von Pathogenen aufgestellt, die schwere weltweite Epidemien in der näheren Zukunft auslösen könnten, und gegen die eine Impfstoffherstellung prioritär ist. Dieses sind aktuell (Stand: März 2020):
SARS-CoV-2, verantwortlich für COVID-19
Krim-Kongo-Hämorrhagisches-Fieber-Virus
Filoviren wie das Ebolavirus oder das Marburg-Virus
Lassafieber
neu entstehende humanpathogene hoch-infektiöse Coronaviren wie MERS-CoV oder das SARS-assoziierte Coronavirus
das Nipah- und Hendra-Virus
Rifttalfieber-Virus (auch rift valley fever virus)
Zikavirus
Disease X
Um eine globale Antwort auf die Herausforderungen geben zu können, rief Stanley Plotkin 2015 dazu auf, die bestehenden Impfforschungskampagnen zu koordinieren und einen Finanzierungsrahmen für die Forschung und Entwicklung neuer Impfstoffe zu schaffen. Diese Initiative wurde auch vom 2015er Konsensus der Oslo consultation on financing of R&D prepraedness and response to epidemic emergencies der WHO unterstützt.
Darüber hinaus unterstützt CEPI die Entwicklung von Vakzinierungsplattformen, die eine schnelle Bereitstellung von Impfstoffen gegen bisher unbekannte Pathogene und durch diese ausgelöste bisher unbekannte Erkrankungen (Disease X) ermöglichen.
Gründung und Organisation
Start beim Weltwirtschaftsforum 2017 in Davos
Auf dem Weltwirtschaftsforum im Januar 2016 in Davos kam es dann zum Beschluss, eine Initiative zur Impfstoffentwicklung zu gründen. Der Auftrag ist, die Entwicklung von Impfstoffen zu stimulieren, zu finanzieren und zu koordinieren. Um diese Herausforderung umzusetzen, wurden im Frühjahr 2016 drei Expertenteams (Task teams) gebildet, die für die erste Phase die Prioritäten festlegten:
Orientierung an der Prioritätenliste der WHO für die Impfstoffentwicklung
Investitionen in den Lücken der derzeitigen Impfstoffentwicklung, und insbesondere Förderung der späten vorklinischen Studien mit dem Proof of Concept, und Förderung von Phase-II-Studien.
Unterstützung technischer und institutioneller Plattformen, die bei neu auftretenden Epidemien rasch handeln und Impfstoffe entwickeln können, mit der Entwicklung von Partner-Netzwerken.
In der Start-up-Phase wurde dann CEPI als internationale Non-Profit-Organisation durch die Regierungen von Norwegen, Indien, dem britischen Wellcome Trust, dem Weltwirtschaftsforum und der Bill-und-Melinda-Gates-Stiftung am 19. Januar 2017 auf dem Weltwirtschaftsforum in Davos gegründet, und Stakeholder wurden eingeladen, beizutreten. Über deren Ausgestaltung berieten CEPI-Vertreterinnen und Vertreter am 11. und 12. Juli 2017 im Bundesministerium für Bildung und Forschung. Deutschland ist Gründungsmitglied der Impfstoff-Initiative. Mehr als 80 Organisationen und über 200 Privatpersonen haben daraufhin ihr Interesse bekundet. Es wurden dann ein vorläufiges Sekretariat gegründet, mit Büros (functional nodes) in Norwegen, Indien und Großbritannien, darüber hinaus ein vorläufiger Vorstand unter Führung durch John-Arne Røttingen vom norwegischen Public Health-Institut benannt, ein vorläufiger Aufsichtsrat unter K. VijayRaghavan vom indischen Department of Biotechnology und ein vorläufiges wissenschaftliches Komitee unter Leitung von Mark Feinberg, dem Vorsitzenden der Internationalen AIDS-Impf-Initiative eingerichtet. Im Aufsichtsrat sitzt auch die stellvertretende Generalsekretärin der Generaldirektion Forschung und Innovation der EU-Kommission, Ruxandra Draghia-Akli. Ein erster Geschäftsplan sah für die ersten fünf Jahre ein Budget von einer Milliarde Dollar vor, die durch Zusagen von Geldgebern gesichert sind.

Curevac
Die Curevac AG (Eigenschreibweise CureVac) mit Sitz in Tübingen ist ein biopharmazeutisches Unternehmen, das sich auf die Erforschung und die Entwicklung von Arzneimitteln auf der Grundlage des Botenmoleküls messenger RNA (mRNA) spezialisiert hat.
Geschichte
2000 wurde Curevac an der Universität Tübingen aus den Arbeitskreisen von Hans-Georg Rammensee und Günther Jung gegründet. 2003 zog das Unternehmen mit 18 Mitarbeitern ins Biotechnologiezentrum Tübingen. Im selben Jahr wurde zum weltweit ersten Mal ein Krebspatient in Tübingen direkt mit mRNA behandelt 2006 erhielt Curevac die Genehmigung für die erste GMP-Produktionsstätte. Seit 2013 veranstaltet Curevac jährlich die International mRNA Health Conference in Tübingen. Gemeinsam mit dem Museum der Universität Tübingen eröffnete Curevac 2015 eine Dauerausstellung im Tübinger Schlosslabor.
Im Mai 2018 wechselte Gründer und Vorstandsvorsitzender Ingmar Hoerr in den Vorsitz des Aufsichtsrats. Daniel L. Menichella, zuvor Chief Business Officer und Chief Executive Officer der US-amerikanischen Curevac-Tochter, wurde zum neuen Vorstandsvorsitzenden ernannt.
Im Februar 2019 gaben internationalen Impfstoffallianz CEPI und Curevac eine Vereinbarung in Höhe von 34 Mio. US-Dollar zur weiteren Entwicklung von Curevacs Vakzinierungsplattform bekannt. Die Plattform soll eine schnelle Versorgung mit RNA-Impfstoffen gegen bekannte Erkrankungen wie Lassafieber, Gelbfieber und Tollwut ermöglichen.
Ende Januar 2020 erhielt Curevac von CEPI eine weitere Förderung in Höhe von bis zu 8,3 Mio. Euro für die beschleunigte Impfstoffentwicklung und -herstellung sowie für klinische Studien gegen das kurz zuvor erstmals aufgetretene Coronavirus SARS-CoV-2, das bald darauf weltweit die COVID-19-Pandemie verursachte. Anfang März 2020 begannen Versuche an Mäusen. Von zunächst sieben Varianten wurden zunächst vier und anschließend zwei weiterverfolgt. Die beiden Varianten befinden sich in Produktion und sollen ab Frühsommer klinischen Tests unterzogen werden, um die Variante mit der besten Wirkung zu finden (Stand: 20. März 2020). Im Juni 2020 sollen Versuche am Universitätsklinikum Tübingen beginnen. Anschließend steht ein Zulassungsprozess an. Ein breit zur Verfügung stehender Impfstoff könnte Anfang 2021 verfügbar sein (Stand: April 2020). Das Unternehmen arbeite an einer Weiterentwicklung der Produktionskapazität, um ggf. Milliarden von Impfdosen herstellen zu können.
Aufgrund der COVID-19-Pandemie traf sich am 2. März 2020 der damalige Vorstandsvorsitzende Menichella mit US-Präsident Donald Trump. Trump habe sich dabei bemüht, die Rechte an dem Impfstoff exklusiv für die USA zu sichern und wissenschaftliche Mitarbeiter abzuwerben. Am 11. März 2020 übernahm Hoerr erneut den Vorstandsvorsitz. Am 15. März 2020 gab Curevac bekannt, dass ein möglicher SARS-CoV-2-Impfstoff nicht einer Nation, sondern der ganzen Welt zur Verfügung stehen soll. Mehrheitseigner Dietmar Hopp sagte: „Für mich ist das selbstverständlich, es kann gar nicht sein, dass eine deutsche Firma den Impfstoff entwickelt und dieser in den USA exklusiv genutzt wird. Das war für mich keine Option.“ Er ergänzte, dass er persönlich nicht mit Trump gesprochen habe. Am 16. März 2020 dementierte Curevac die Presseberichte und erklärte, Curevac habe weder vor noch während noch nach dem Treffen der Task Force im Weißen Haus am 2. März ein Angebot von der US-Regierung oder verwandten Stellen erhalten. Ebenfalls am 16. März teilte das Unternehmen mit, dass der seit wenigen Tagen wieder amtierende Vorstandsvorsitzende Hoerr krankheitsbedingt für gewisse Zeit abwesend sei und seine Rolle daher nicht ausüben könne.
Finanzierung
Curevac wurde von 2006 bis 2014 alleinig von der dievini Hopp BioTech holding, einer Biotech-Venture Capital-Gesellschaft von SAP-Gründer Dietmar Hopp, finanziert, darunter 80 Mio. Euro im September 2012. Das Kapital von Curevac wuchs durch dieses Investment auf insgesamt 145 Mio. Euro; Hopp war zu dem Zeitpunkt damit zu rund 90 % an Curevac beteiligt.
Im Februar 2015 wurde die Bill & Melinda Gates Foundation als neuer Investor gewonnen und im Oktober 2015 wurde ein Private Placement mit fünf weiteren Investoren (Baillie Gifford, Chartwave Ltd., Coppel Familie, Northview und Sigma Group) und einem Volumen von 98,7 Mio. Euro durchgeführt. Dabei investierte die Bill & Melinda Gates Foundation 52 Mio. Dollar in CureVac.
Im Jahr 2016 erbrachte die dievini Hopp BioTech holding eine weitere Einzahlung von 20,7 Mio. Euro. 2016 wurden im Zuge einer weiteren Kapitalerhöhung zwei neue Investoren, die baden-württembergische Investitionsbank L-Bank und die Baden-Württembergische Versorgungsanstalt für Ärzte, Zahnärzte und Tierärzte, hinzugewonnen, die insgesamt 26,5 Mio. Euro investierten. 2017 erfolgte eine weitere Kapitalerhöhung unter Beteiligung des US-Pharmakonzerns Eli Lilly & Co. in Höhe von 45,0 Mio. Euro. Seit ihrer Gründung im Jahr 2000 hat die Curevac über die Ausgabe von Anteilen über 360 Mio. Euro eingeworben.
Im Juni 2020 gab die Bundesregierung bekannt, dass die staatseigene Förderbank KfW sich ab sofort mit 300 Millionen Euro an Curevac beteiligen wird. Die KfW wird damit einen Anteil von etwa 23 Prozent an CureVac halten. Das Unternehmen wird damit mit ca. 1,3 Mrd. Euro bewertet.
Standorte
Neben dem Hauptsitz in Tübingen hat Curevac einen Standort in Frankfurt am Main, wo an der klinischen Entwicklung gearbeitet wird. Eine US-amerikanische Tochtergesellschaft ist seit 2015 in Boston aktiv.
Forschungsgebiete
Curevac ist auf drei Forschungsgebieten aktiv.
In der Onkologie konzentriert sich Curevac auf neue therapeutische Ansätze zur Behandlung solider Tumoren durch den Einsatz von sequenz-optimierter mRNA („RNActive“). Weltweit zum ersten Mal wurden in Phase-I/IIa-Studien in mehreren Ländern (Italien, Schweiz, Deutschland und USA) in den Indikationen Prostatakrebs und Lungenkrebs Patienten mit mRNA behandelt. Für Patienten mit kastrationsresistentem Prostatakrebs wurde im März 2013 eine randomisierte klinische Phase-IIb-Studie mit bis zu 200 Patienten in mehreren europäischen Ländern begonnen. Im September 2014 vereinbarten Boehringer Ingelheim und Curevac eine Kooperation zur Weiterentwicklung des Wirkstoffs CV9202 (BI 1361849), einem therapeutischen Impfstoff von Curevac zur Behandlung des nichtkleinzelligen Bronchialkarzinoms (NSCLC).
Curevac entwickelt auf mRNA-Grundlage prophylaktische Impfstoffe gegen Infektionen. Hier kooperiert man mit Sanofi-Pasteur (Sanofi-Aventis-Gruppe), einem der Weltmarktführer für Impfstoffe. Darüber hinaus entwickelt Curevac ein Immunstimulans (Adjuvans) auf RNA-Basis zur Verstärkung der Wirkung von prophylaktischen und therapeutischen Impfstoffen. Im November 2012 hat Curevac zusammen mit dem Friedrich-Loeffler-Institut in der Zeitschrift Nature Biotechnology Daten zu einem mRNA-basierten Grippeimpfstoff veröffentlicht. Dieser Impfstoff könnte einen lebenslangen Schutz bewirken; er muss noch in umfangreichen klinischen Studien getestet werden. Im Oktober 2013 sind Curevac und das Pharmaunternehmen Johnson & Johnson eine Kooperation zur Entwicklung eines Grippeimpfstoffes eingegangen.
Im Bereich der molekularen Therapien arbeitet Curevac unter anderem mit Arcturus Therapeutics zusammen, um Wirkstoffe gegen seltene Krankheiten wie das Defizit an Ornithin-Transcarbamylase zu entwickeln.
Auszeichnungen
Im Jahr 2007 erhielt Curevac den Innovationspreis des Landes Baden-Württemberg und war ebenso Preisträger des bundesweiten Weconomy-Wettbewerbes, der gemeinsam vom Handelsblatt und der Wissensfabrik vergeben wird. Ebenfalls erhielt Curevac zusammen mit dem Forschungspartner NMI den bundesweiten Kooperationspreis der VBU DECHEMA für neuartige Ansätze zur Immuntherapie.
Am 10. März 2014 erhielt Curevac den erstmals verliehenen und mit 2 Mio. Euro dotierten Innovationspreis der Europäischen Kommission für eine neue Impftechnologie auf Basis der mRNA.

AstraZeneca
AstraZeneca ist ein internationaler Pharmakonzern, der 1999 aus der schwedischen Astra AB und der britischen Zeneca PLC entstand. Zeneca war 1993 aus der Pharmasparte des britischen Chemieunternehmens Imperial Chemical Industries entstanden. Der Hauptsitz ist in London, die Entwicklungs- und Forschungsabteilung sitzt im schwedischen Södertälje südlich von Stockholm. AstraZeneca ist 2018 mit 22,09 Milliarden US-Dollar Umsatz und 64.600 Mitarbeitern einer der größten Arzneimittelhersteller weltweit.
Standorte in Deutschland
In Deutschland unterhält AstraZeneca einen Standort in Wedel bei Hamburg mit ca. 625 Mitarbeitern im Innen- und Außendienst. Aufgrund veränderter wirtschaftlicher und gesundheitspolitischer Rahmenbedingungen erfolgte 2012 ein Abbau von ca. 400 Stellen. Im September 2019 kündigte AstraZeneca zudem an den Produktionsstandort Wedel Ende 2021 zu schließen. Als Grund für die Schließung gab AstraZeneca Rückgänge bei Tablettenverpackungen nach Produktverkäufen und eine zunehmende Konzentration auf Spezialpräparate mit kleineren Volumen an.
AstraZeneca unterhielt einen Standort in Plankstadt in Baden-Württemberg mit rund 430 Mitarbeitern. Am 26. April 2007 wurde bekanntgegeben, dass der Standort Plankstadt bis 2009 verkauft oder geschlossen wird.[6] Der Standort wurde an die International Chemical Investors Group verkauft und firmiert seit dem 1. Februar 2008 unter dem Namen Corden Pharma.
Firmenbeteiligungen
Am 2. Dezember 1999 wurde bekanntgegeben, dass die Agrarbereiche von Novartis und AstraZeneca ausgegliedert und zum weltgrößten Agrarkonzern Syngenta mit Firmensitz in Basel fusioniert werden. Im Dezember 2013 gab AstraZeneca die Übernahme der Diabetes-Sparte von Bristol-Myers Squibb zum Preis von 2,7 Milliarden US-Dollar nebst Meilensteinzahlungen in Höhe von 1,6 Milliarden US-Dollar bekannt. Nachdem im Laufe des Jahres 2014 ein Übernahmeversuch des Unternehmens durch Pfizer abgelehnt worden war, expandierte AstraZeneca im Juli 2014 mit der Übernahme der Atemwegssparte des spanischen Wettbewerbers Almirall für 1,22 Milliarden US-Dollar inklusive Meilensteinzahlungen selbst. Im Februar 2015 gab das Unternehmen schließlich bekannt, auch die Rechte an den von Almirall gekauften Atemwegsprodukten in den USA und Kanada von Actavis zum Preis von 700 Millionen US-Dollar inklusive Meilensteinzahlungen zu übernehmen. Der US-Pharmakonzern Pfizer hat den Kauf großer Teile des Antibiotika-Geschäfts von AstraZeneca angekündigt.

Pfizer
Die Pfizer Inc. [ˈfaɪzəɹ], ursprüngliche Aussprache [ˈpfiːtsəɹ], ist ein weltweit vertretener Pharmakonzern mit Hauptsitz in New York City, New York, Vereinigte Staaten. Gegründet wurde er von Charles Pfizer (eigentlich Karl Pfizer) aus Ludwigsburg. Pfizer ist – nach Roche – das zweitgrößte Pharmaunternehmen der Welt, gefolgt von Novartis. Der Umsatz von 51,8 Mrd. USD im Jahr 2019 bedeutet ein Rückgang gegenüber Vorjahr von 1 Prozent.
Hauptwachstumspräparate sind: Ibrance (Palbociclib), Eliquis (Apixaban), Xeljanz (Tofacitinib) und Vyndaqel (Tafamidis).
Geschichte
Die Charles Pfizer & Company wurde von Karl Pfizer und Charles Erhart 1849 in Brooklyn, New York gegründet. Das erste Produkt war Santonin, ein Mittel gegen Parasiten. Die Firma war sehr erfolgreich und erweiterte sich in den folgenden Jahren um weitere Produktionsstätten, Verwaltungs- und Lagerhäusern in New York. 1951 wurden weltweit neue Werke aufgebaut; unter anderem in Belgien, Brasilien, Puerto Rico, Kanada, Kuba und England. 1952 folgte Pfizer mit dem Aufbau einer Agrarsparte und spezialisierte sich ab 1953 durch Übernahme der J.B. Roerig & Co. auf Nahrungsergänzungsmittel. 1971 erfolgte die Übernahme des deutschen Pharmaherstellers Heinrich Mack in Illertissen.
1996 wurden neue Antibiotika an Kindern in Nigeria während einer schweren Meningitis-Epidemie getestet, ohne dass hierfür ausreichende Genehmigungen vorlagen; elf von ihnen starben. Pfizer wurde nach dem Bekanntwerden in New York 2007 von der nigerianischen Provinz Kano verklagt. Die außergerichtliche Einigung 2009 wurde von den Familien der Opfer wegen der Gentests, mit denen ermittelt werden sollte, wer Anspruch auf Entschädigung hat, abgelehnt. Nachdem der Oberste Gerichtshof der Vereinigten Staaten im Juni 2010 einen Einspruch von Pfizer abwies, ist der Weg für einen Prozess in den Vereinigten Staaten frei.
2000 wurden die Pharmageschäfte durch die Übernahme von Warner-Lambert (inkl. des Fertigungsstandortes Gödecke) in Freiburg für 116 Milliarden Dollar ausgeweitet, die Aquaristik-Sparte 2002 durch den Verkauf von Tetra abgestoßen. Nach der Übernahme von Pharmacia 2003 wurde 2006 die Consumer-Sparte an Johnson & Johnson verkauft.
Zur Einsparung von bis zu 1,5 Mrd. Euro wurde am 21. Januar 2007 der Abbau von 10.000 Arbeitsplätzen angekündigt. Am 7. Juni 2008 folgte die Ankündigung der Verlegung der Deutschlandzentrale von Karlsruhe nach Berlin.
Es folgten weitere Übernahmen (2009: Wyeth, 2010: Whitehall-Much, 2015: Hospira), Verkäufen (2012: die Babynahrungssparte an den Nestlé-Konzern, 2013: die Tiergesundheitssparte (seither Zoetis)) und die Gründung eines Joint-Ventures für HIV-Medizin mit GlaxoSmithKline 2009.
Im November 2015 kündigten Pfizer und Allergan ihren Zusammenschluss zur Pfizer plc mit neuem Hauptsitz in der steuerlich deutlich günstigeren irischen Hauptstadt Dublin an (tax inversion). Pfizer sollte für die Übernahme durch die kleinere Allergan (reverse takeover) im Wege eines Aktientauschs rund 160 Milliarden Dollar zahlen, was die bis dahin größte Übernahme in der Geschichte der Pharmabranche dargestellt hätte. Mit einem Umsatz von dann 60 Milliarden Dollar wäre Pfizer wieder der größte Arzneimittelhersteller der Welt geworden. Im April 2016 gab jedoch Pfizer bekannt, dass man die beabsichtigte Fusion aufgrund stark verschärfter US-Steuergesetze doch nicht weiterverfolgte. Obwohl die ursprünglichen Vereinbarungen für diesen Fall eine Vertragsstrafe von 400 Millionen USD vorsahen, einigte man sich auf eine Zahlung von 150 Millionen USD von Pfizer an Allergan.
Weil Pfizer ein Epilepsie-Medikament in Großbritannien 2600 % zu teuer verkauft hat, ist der Konzern zu einer Strafe von 100 Millionen € verurteilt worden. Pfizer will gegen das Urteil Berufung einlegen.
Verfahren gegen Pfizer in Nigeria und den USA
Laut Angaben nigerianischer Behörden und verschiedener Organisationen testete Pfizer im Jahr 1996 das mittlerweile verbotene Antibiotikum Trovafloxacin (Trovan) an etwa 200 Kindern aus dem Umkreis von Kano (Nigeria). Durch die Wirkung des zuvor noch nicht am Menschen erprobten Mittels starben fünf Kinder, weitere erlitten Schäden. Zahlreichen Kindern wurde im Rahmen dieser Studie der Zugang zu einem erwiesenermaßen wirksamen Medikament vorenthalten.
Diese Thematik wird in dem Roman Der ewige Gärtner von John le Carré (und der gleichnamigen Verfilmung von Fernando Meirelles) aufgegriffen und verarbeitet.
Der oberste Gerichtshof in den USA ebnete im Juni 2010 die Wege für ein Entschädigungsverfahren, nachdem eine außergerichtliche Einigung zwischen Pfizer und dem Bundesstaat Kano von den Opfern abgelehnt wurde.
Der deutsche Kinderarzt und Infektiologe Juan Walterspiel, der damals bei Pfizer die pädiatrischen Studien leitete, hatte schwerwiegende Kritik an der Planung und Durchführung der Versuche geübt und eine weitere Mitarbeit verweigert. Daraufhin wurde ihm gekündigt. Ein Gerichtsverfahren wurde von der Washington Post aufgegriffen, die die Studie und ihre Fragwürdigkeit thematisierte. Pfizer besteht darauf, dass Walterspiel aus anderen, nicht genannten Gründen gekündigt worden sei und dass die Studie ethischen Normen entspreche. Zurzeit laufen mehrere Verfahren in Nigeria mit zum Teil erheblichen Schadensersatzforderungen. Zwei weitere Klagen sind von nigerianischen Eltern in den USA eingereicht worden. Die Verfahren sind im Januar 2009 in New York wieder aufgenommen worden.
Im Dezember 2010 wurden von WikiLeaks Dokumente veröffentlicht, nach denen Pfizer auch versucht hatte, den nigerianischen Staatsanwalt unter Druck zu setzen, um hohen Strafzahlungen zu entgehen.
Am 2. September 2009 bestätigte das Unternehmen die Zahlung von 2,3 Milliarden Dollar, um damit einen Streit mit der US-Regierung über unlautere Werbepraktiken zu beenden. Es ging unter anderem um die Werbung für das verschreibungspflichtige Schmerzmittel Bextra. Nach Berichten über starke Nebenwirkungen hatte das Unternehmen das Arzneimittel 2005 vom Markt genommen. Mit dem Vergleich werden auch zivil- und strafrechtliche Vorwürfe rechtswidriger Werbepraktiken im Zusammenhang mit den Medikamenten Zyvox, Geodon und Lyrica beigelegt.
Pfizer und BioNTech entwickeln Impfstoffkandidaten gegen COVID-19
Die Unternehmen entwickeln gemeinsam den mRNA-basierten Impfstoff-Kandidaten BNT162 von BioNTech zur Vorbeugung einer COVID-19 Infektion
Im Rahmen der Zusammenarbeit bündeln die Unternehmen ihre Expertise und Ressourcen, um die Entwicklung von BNT162 zu beschleunigen
Basis der Zusammenarbeit ist eine Vereinbarung der Unternehmen aus dem Jahr 2018 zur gemeinsamen Entwicklung eines mRNA-basierten Grippe-Impfstoffes
New York und Mainz, 17. März 2020. Pfizer Inc. (NYSE: PFE, “Pfizer”) und BioNTech SE (Nasdaq: BNTX, “BioNTech”) haben eine Absichtserklärung zur gemeinsamen Entwicklung und Distribution (exkl. China) eines mRNA-basierten Coronavirus-Impfstoff-kandidaten verabschiedet, der eine COVID-19 Infektion verhindern soll. Die Unternehmen haben einen Material-Transfer und einen Kooperationsvertrag realisiert, der es ihnen ermöglicht, ihre Zusammenarbeit sofort zu beginnen.
Ziel der Zusammenarbeit ist die beschleunigte Entwicklung von BioNTechs potenziellem COVID-19 mRNA Impfstoffprogramm, BNT162, das voraussichtlich Ende April in die klinische Testung gehen soll. Das schnelle Voranschreiten des Vorhabens baut auf der bestehenden Zusammenarbeit in der Forschung und Entwicklung auf, die Pfizer und BioNTech 2018 begonnen haben, um gemeinsam mRNA-basierte Grippe-Impfstoffe zu entwickeln.
„Wir freuen uns, dass die erfolgreiche Beziehung zwischen Pfizer und BioNTech es beiden Unternehmen ermöglicht, unsere Ressourcen im Angesicht dieser globalen Herausforderung schnell zu mobilisieren,” sagt Mikael Dolsten, Chief Scientific Officer und President, Worldwide Research, Development & Medical, Pfizer. „Wir wollen unser Engagement gegen die Pandemie untermauern, indem wir unsere Kenntnisse in der Entwicklung, im regulatorischen Umfeld und in der Vermarktung von Arzneimitteln mit der mRNA-Impfstoff-Technologie von BioNTech kombinieren.“
„Eine globale Pandemie erfordert globales Engagement. Wir bündeln mit unserem Partner Pfizer die Kräfte, um unsere Bemühungen beschleunigen, einen COVID-19 Impfstoff weltweit für Betroffene verfügbar zu machen“, sagte Ugur Sahin, Mitgründer and CEO von BioNTech.
Die Unternehmen planen, für die gemeinsamen Aktivitäten mehrere Forschungsstandorte beider Unternehmen in den USA und in Deutschland zu nutzen. Die Zusammenarbeit der Unternehmen beginnt sofort. Innerhalb der nächsten Wochen finalisieren Pfizer und BioNTech die Details der Vereinbarung in Bezug auf die finanziellen Bedingungen, sowie auf alle Aktivitäten der Entwicklung, Produktion und potenziellen Vermarktung.
Am 13. März 2020 rief Pfizer die Pharma-Industrie in einem Fünf-Punkte-Plan dazu auf, sich im Kampf gegen COVID-19 einer neuen Dimension der Zusammenarbeit zu verpflichten.
Pfizer – Breakthroughs that change patients’ lives
Wenn Menschen krank werden, können sich viele Dinge für sie verändern – ein oft schwieriger Weg beginnt. Bei Pfizer arbeiten weltweit mehr als 10.000 ForscherInnen und insgesamt mehr als 90.000 MitarbeiterInnen daran, sie auf diesem Weg zu unterstützen. Sie entwickeln, produzieren und vertreiben innovative Medikamente und Impfstoffe, die das Leben von PatientInnen verlängern und verbessern.
Hauptsitz von Pfizer ist in New York. In Deutschland sind mehr als 2.500 MitarbeiterInnen an drei Standorten tätig: Berlin, Freiburg und Karlsruhe. Das Werk in Freiburg ist Vorreiter in Sachen Nachhaltigkeit und Industrie 4.0.
Über BioNTech
Biopharmaceutical New Technologies (BioNTech) ist ein Immuntherapie-Unternehmen der nächsten Generation, das bei der Entwicklung von Therapien für Krebs und andere schwere Krankheiten Pionierarbeit leistet. Das Unternehmen kombiniert bahnbrechende Immunologieforschung, moderne therapeutische Plattformen und Bioinformatik-Tools, um die Entwicklung neuartiger Biopharmazeutika rasch voranzutreiben. Das diversifizierte Portfolio an onkologischen Produktkandidaten umfasst individualisierte Therapien sowie off-the-shelf-Medikamente auf mRNA-Basis, innovative chimäre Antigenrezeptor (CAR)-T-Zellen, bispezifische Checkpoint-Immunmodulatoren, zielgerichtete Krebsantikörper und Small Molecules. Auf Basis seiner umfassenden Expertise bei der Entwicklung von mRNA-Impfstoffen und unternehmenseigener Herstellungskapazitäten entwickelt BioNTech neben seiner vielfältigen Onkologie-Pipeline gemeinsam mit Kollaborationspartnern verschiedene mRNA-Impfstoffkandidaten für eine Reihe von Infektionskrankheiten. BioNTech arbeitet Seite an Seite mit weltweit renommierten Kooperationspartnern aus der pharmazeutischen Industrie, darunter Eli Lilly and Company, Genmab, Sanofi, Bayer Animal Health, Genentech (ein Unternehmen der Roche Gruppe), Genevant, Fosun Pharma und Pfizer.
Eine Schlüsselrolle im Geschehen trägt das Unternehmen CordenPharma https://www.cordenpharma.com/ und INTERNATIONAL CHEMICAL INVESTORS S.E. https://ic-investors.com/

Monitoring and Control
We have developed effective planning and controlling tools customized for the chemical and pharmaceutical industries and modified to meet the specific requirements of each of our businesses. We believe that a systematic planning process linked to continuous production, marketing and financial reporting in combination with rigorous cash management tools instils the necessary discipline and focus required to run successful businesses in highly competitive markets.
CordenPharma – AstraZeneca plc
AstraZeneca plc is a British-Swedish multinational pharmaceutical and biopharmaceutical company with its global headquarters in Cambridge, England. Its R&D is concentrated in Cambridge, Gaithersburg, Maryland, and Mölndal in Sweden. AstraZeneca has a portfolio of products for major disease areas including cancer, cardiovascular, gastrointestinal, infection, neuroscience, respiratory and inflammation.
The company was founded in 1999 through the merger of the Swedish Astra AB and the British Zeneca Group (itself formed by the demerger of the pharmaceutical operations of Imperial Chemical Industries in 1993). Since the merger it has been among the world’s largest pharmaceutical companies and has made numerous corporate acquisitions, including Cambridge Antibody Technology (in 2006), MedImmune (in 2007), Spirogen (in 2013) and Definiens (by MedImmune in 2014).
AstraZeneca has a primary listing on the London Stock Exchange and is a constituent of the FTSE 100 Index. It has secondary listings on the New York Stock Exchange and the OMX exchange.
Formed as the global pharmaceutical service & manufacturing platform of International Chemical Investors Group in 2006, CordenPharma is your full-service partner in the Contract Development & Manufacturing (CDMO) of APIs, Drug Products, and associated Packaging Services. Through a growing network of cGMP facilities across Europe and the US organized under five Technology Platforms – Peptides, Lipids & Carbohydrates – Highly Potent & Oncology – Injectables – Small Molecules – Antibiotics – CordenPharma experts translate complex processes, ideas and projects at any stage of development into high-value products.
Coronavirus (COVID-19) response
In March 2020, the company announced that it would be donating PPE, including 9 million face masks, to help support various international health organisations mitigating the COVID-19 pandemic.
In April, the Chief Executive, Pascal Soriot, reported that the company was working with GlaxoSmithKline and the University of Cambridge to develop a new laboratory capable of conducting 30,000 Covid-19 tests per day. The company also announced plans for a clinical trial to assess the potential use of Calquence in the treatment of Covid-19.
In June 2020, the National Institute of Allergy and Infectious Diseases (NIAID) confirmed that the third phase of testing for potential vaccines developed by Oxford University and AstraZeneca would begin in August 2020.
In June 2020, AstraZeneca and Emergent BioSolutions signed a $87 million deal to manufacture doses of the Oxford University’s adenovirus-based COVID-19 vaccine specifically for the U.S. market. The deal was part of the President Trump administration’s Operation Warp Speed initiative to develop and rapidly scale production of targeted vaccines before the end of 2020. Catalent will be responsible for the finishing and packaging process.
On 13 June 2020, AstraZeneca signed a contract with Europe’s Inclusive Vaccines Alliance,a group formed by France, Germany, Italy and the Netherlands, to supply up to 400 million doses of its experimental COVID-19 vaccine to all European Union member states.
facts about vaccine for Covid19 and mRNA
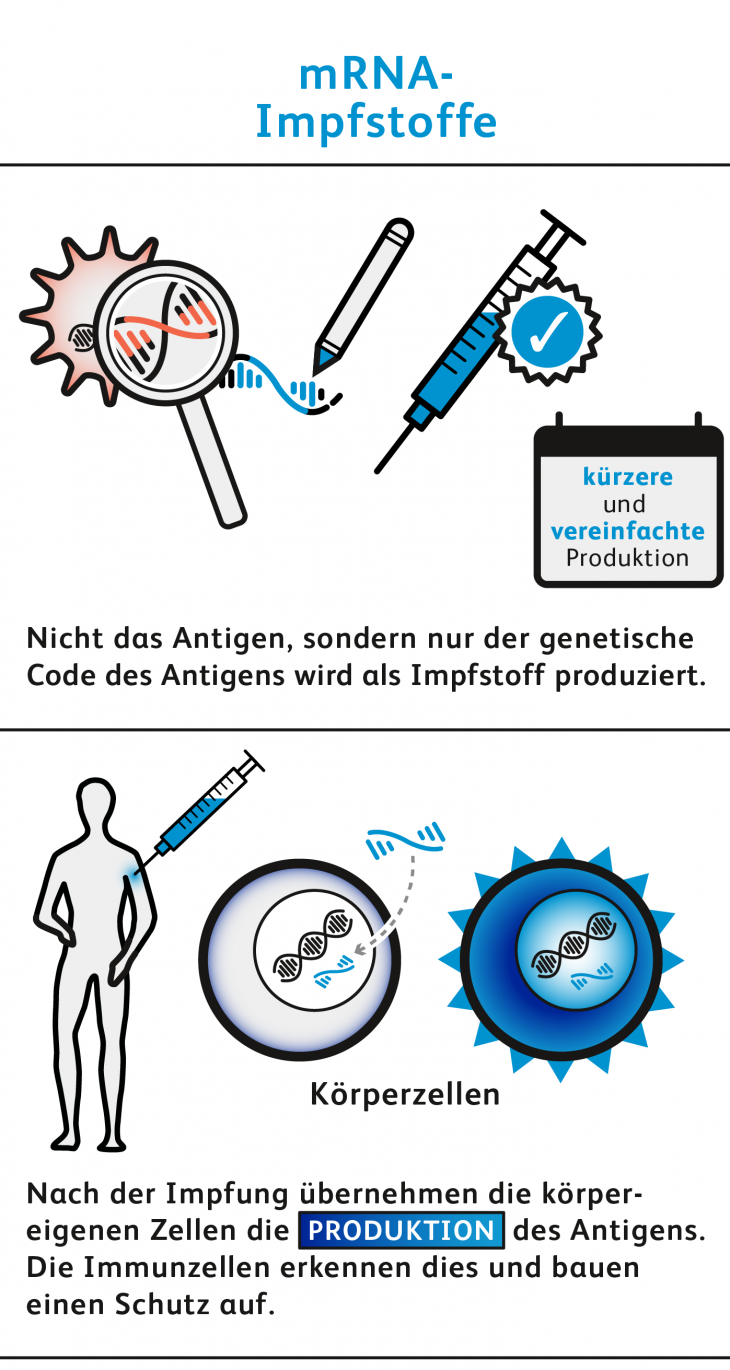
Verwendung von RNA Impfstoff
RNA wird für unterschiedliche Zwecke verwendet. Bei Ribozymen besitzt die RNA eine enzymatische Aktivität, während Aptamere eine längerfristige Bindung an eine Zielstruktur eingeht. Kurze doppelsträngige RNA in Form von siRNA und shRNA wird zur temporären Unterdrückung der Genexpression per RNA-Interferenz verwendet. RNA-Impfstoffe gehören zu den genetischen Impfstoffen, bei denen das Antigen innerhalb der Zellen des Geimpften hergestellt wird.
Ribonukleinsäure (Ri|bo|nu|kle|in|säu|re; kurz RNS; englisch RNA für ribonucleic acid) (lat.-fr.-gr. Kunstwort) ist eine Nukleinsäure, die sich als Polynukleotid aus einer Kette von vielen Nukleotiden zusammensetzt. Das Biomolekül ist bei bestimmten Virentypen (RNA-Viren, Retroviren) sowie den hypothetischen urzeitlichen Ribozyten Träger der Erbinformation, also die materielle Basis der Gene. Das Wort setzt sich zusammen aus Ribose und Nukleinsäure.
Eine wesentliche Funktion der RNA in der biologischen Zelle ist die Umsetzung von genetischer Information in Proteine (siehe Proteinbiosynthese, Transkription und Translation), in Form der mRNA fungiert sie hierbei als Informationsüberträger. Daneben erfüllen spezielle RNA-Typen weitere Aufgaben; bei RNA-Viren macht sie sogar das Genom selbst aus. Weiterhin bestehen auch Teile der für die Umsetzung dieser Information verantwortlichen Zellbestandteile aus RNA: Bei der Reifung der mRNA sind snRNA und snoRNA beteiligt, die katalytischen Bestandteile der Ribosomen bildet die rRNA, und die tRNA transportiert die Bausteine für die Proteine. Ferner sind spezielle RNAs an der Genregulation beteiligt.
RNS kann auch Aufgaben von Enzymen übernehmen (Ribozym) oder ähnlich Antikörpern wirken (Aptamer).
Aufbau und Unterschied zur DNA
RNA und DNA im Vergleich
Vom Aufbau her ist die RNA der DNA ähnlich. RNA-Moleküle sind – im Gegensatz zur doppelsträngigen DNA – in der Regel einzelsträngig, können allerdings in kurzen Strecken mit komplementären Basensequenzen (A-U, G-C) charakteristische Rückfaltungen ausbilden, die intramolekular den Eindruck einer Doppelstrang-Helix erwecken. Beide sind Polynukleotide, bei denen die Nukleobasen an Zuckern über Phosphorsäurediester miteinander verknüpft sind. Die Einzelsträngigkeit erhöht die Zahl der Möglichkeiten für dreidimensionale Strukturen der RNA und erlaubt ihr chemische Reaktionen, die der DNA nicht möglich sind. Jedes Nukleotid besteht bei der RNA aus einer Ribose (d. h. einer Pentose: einem Zucker mit fünf C-Atomen), einem Phosphatrest und einer organischen Base. Die Ribose der RNA ist mit derjenigen der DNA identisch, bis auf eine Hydroxygruppe statt eines Wasserstoff-Atoms an der 2′-Position im Pentose-Ring (daher auch Desoxyribonukleinsäure, DNA). Dieser Unterschied macht die RNA weniger stabil im Vergleich zur DNA, da er eine Hydrolyse durch Basen ermöglicht: Die OH-Gruppe an der 2′-Position des Zuckers wird durch ein negativ geladenes Hydroxidion einer Base ihres Protons beraubt und der dann zurückgebliebene Sauerstoff geht eine Ringbindung mit dem Phosphor ein, wodurch die Bindung zum nächsten Nukleotid gelöst wird. Die RNA wird so in ihre Nukleotide zerlegt.
In der RNA kommen die folgenden organischen Basen vor: Adenin, Guanin, Cytosin und Uracil. Die ersten drei Basen kommen auch in der DNA vor. Uracil dagegen ersetzt Thymin als komplementäre Base zu Adenin. Vermutlich nutzt RNA Uracil, da dieses energetisch weniger aufwändig herzustellen ist (keine Methyl-Substituierung).
Als Sekundärstrukturen sind bei der RNA vor allem Hairpin-, Stemloop- und Loop-Strukturen bekannt, eine Helix-Konformation ist aber ebenfalls möglich, wobei Hairpin- und Stemloop-Strukturen sowohl Einzelstrang- als auch Doppelstrangbereiche aufweisen. Die Loop-Strukturen bezeichnen einzelsträngige Schlaufenstrukturen innerhalb eines Moleküls.
RNA kann wie DNA ebenfalls als doppelsträngiges Molekül vorliegen. Sie weist dabei die typischen Merkmale einer Watson-Crick-Helix auf: antiparallele Anordnung der RNA-Stränge und rechtsgewundene Helix. Sie nimmt dabei die Form einer A- oder A´-Helix an (siehe DNA). Die A-RNA wird auch als RNA-11 bezeichnet, homolog zur A´-RNA, die als RNA-12 bezeichnet wird. Hierbei gibt die Zahl nach dem Spiegelstrich die Anzahl der Basenpaare je Helixwindung wieder. A´-RNA kommt häufig bei hohen Salzkonzentrationen vor (über 20 %).
A-RNA: 11 Basenpaare pro Helixwindung, Ganghöhe 2,7 nm bis 2,8 nm, Neigungswinkel zur Helixachse ca. 14°
A´-RNA: 12 Basenpaare pro Helixwindung, Ganghöhe 3 nm, Neigungswinkel zur Helixachse 16° bis 19°
Das in Lebewesen vorkommende Enantiomer der RNA ist die D-RNA. Sie ist aus D-Ribonukleotiden aufgebaut. Die Chiralitätszentren liegen in der D-Ribose. Durch Verwendung von L-Ribose, bzw. L-Ribonukleotiden lässt sich L-RNA synthetisieren. Diese ist vergleichsweise stabiler gegenüber dem enzymatischen Abbau durch RNasen.
Synthese von RNA
Das Enzym RNA-Polymerase katalysiert an der DNA durch den Prozess der Transkription aus Nukleosidtriphosphat (NTP) die RNA. Dafür setzt sich die RNA-Polymerase an eine Promotor genannte Nukleotid-Sequenz der DNA (Transkriptionsinitiation). Dann trennt sie die DNA-Doppelhelix durch Lösen der Wasserstoffbrücken in einem kurzen Bereich in zwei DNA-Einzelstränge auf. Am codogenen Strang der DNA lagern sich durch Basenpaarung komplementäre Ribonukleotide an. Sie werden unter Eliminierung eines Pyrophosphat durch eine esterartige Bindung zwischen Phosphorsäure und Ribose miteinander verknüpft. Die Ableserichtung der DNA verläuft vom 3′-Ende zum 5′-Ende, die Synthese der komplementären RNA dementsprechend 5’→3′. Die Öffnung der DNA-Doppelhelix erfolgt nur in einem kurzen Bereich, so dass der bereits synthetisierte Teil der RNA aus dieser Öffnung heraushängt und zwar mit dem 5′-Ende der RNA voran. Die Synthese der RNA wird an einem Terminator genannten DNA-Abschnitt beendet. Danach wird das RNA-Transkript entlassen und die RNA-Polymerase löst sich von der DNA.
RNA kann per Phosphoramidit-Synthese künstlich erzeugt werden.
Biologische Bedeutung
RNA-Moleküle können unterschiedliche Funktionen ausüben. Die RNA kann genetische Information übertragen. Andere RNA-Moleküle tragen zur Übersetzung dieser Information in Proteine bei sowie bei der Regulation der Gene. Darüber hinaus kann RNA auch katalytische Funktionen ähnlich einem Enzym innehaben. RNA wird daher – je nach ihrer Funktion – auch verschieden benannt. Vorangestellte Kleinbuchstaben kennzeichnen die unterschiedlichen RNA-Typen:
Die mRNA, Boten-RNA (engl. messenger RNA) kopiert die in einem Gen auf der DNA liegende Information und trägt sie zum Ribosom, wo mit Hilfe dieser Information die Proteinbiosynthese stattfinden kann. Jeweils drei im Leseraster des Polynukleotidstrang nebeneinander liegende Nukleotide bilden ein Codon, mit dessen Hilfe sich eine spezifische Aminosäure, die in ein Protein eingebaut werden soll, eindeutig bestimmen lässt. Dieser Zusammenhang wurde 1961 von Heinrich Matthaei und Marshall Warren Nirenberg gefunden. Die Entschlüsselung des genetischen Codes markiert einen Neubeginn in fast allen Bio-Wissenschaften.
Die folgenden RNA-Klassen werden allgemein als nichtcodierende Ribonukleinsäuren bezeichnet.
Die asRNA, antisense-RNA, dient der Regulation der Genexpression.
Die circRNA, zirkuläre RNA ist durch Bindung an miRNA an der Regulation beteiligt.
Die hnRNA, heterogene Kern-RNA (engl. heterogeneous nuclear RNA), kommt im Zellkern von Eukaryoten vor und ist eine Vorstufe der reifen mRNA, häufig wird sie daher auch als prä-mRNA (oder engl. pre-mRNA für precursor mRNA) bezeichnet.
Die miRNAs, microRNAs sind eng verwandt mit den siRNAs und dient der Regulation zellulärer Prozesse wie z. B. Proliferation und Zelltod.
Die Riboswitches dienen der Genregulation. Sie können entweder aktivierend oder reprimierend wirken.
Die Ribozyme sind katalytisch aktive RNA-Moleküle. Sie katalysieren wie Enzyme chemische Reaktionen.
Die rRNA, ribosomale RNA, trägt, ähnlich wie die tRNA, keine genetische Information, sondern ist am Aufbau des Ribosoms beteiligt und ist bei der Knüpfung der Peptidbindung auch katalytisch aktiv.
Die saRNA, selbstampflifizierende RNA, wird bei RNA-Impfstoffen verwendet, um die Wirkdauer zu verlängern.
Die siRNA, small interfering RNA, entsteht bei einem Signalweg der Zelle, der als RNAi (RNA Interference) zusammengefasst wird. Dabei wird dsRNA (doppelsträngige RNA; englisch double-stranded RNA) durch das Enzym Dicer in viele kleinere Fragmente von ca. 22 Nukleotiden Länge zerteilt (die siRNAs) und in den Enzymkomplex RISC (RNA-induced silencing complex) eingebaut. Mithilfe der inkorporierten RNA-Fragmente bindet RISC komplementär an DNA, z. B. Genbereiche, oder mRNA und kann diese damit „abschalten“. siRNA’s werden aktuell (2006) intensiv auf ihre Beteiligung an verschiedenen Zellvorgängen und Krankheiten erforscht.
Die shRNA wird zur RNAi verwendet.
Die snoRNA, small nucleolar-RNA, finden sich im Nukleolus, und die eng verwandten scaRNAs in den Cajal Bodies.
Die snRNA, small nuclear-RNA, im Zellkern von Eukaryoten, ist verantwortlich für das Spleißen der hnRNA am Spleißosom.
Die lncRNA, long non-coding RNA, sind länger als 200 Nukleotide und unterscheiden sich dadurch von kleinen regulatorischen RNAs, wie den miRNAs und den siRNAs.[4]
Die piRNA, Piwi-interacting RNA, sind 26–31 Nukleotide lang und unterscheiden sich dadurch von den etwas kleineren miRNAs und siRNAs. Sie bilden Komplexe mit PIWI-Proteinen die am epigenetischen und posttranskriptionellen Silencing in Keimzellen beteiligt sind.[5]
Die tRNA, Transfer-RNA codiert keine genetische Information, sondern dient als Hilfsmolekül bei der Proteinbiosynthese, indem sie eine einzelne Aminosäure aus dem Cytoplasma aufnimmt und zum Ribosom transportiert. Die tRNA wird durch ein bestimmtes RNA-Gen codiert.
Die tracrRNA, die beim CRISPR/Cas9 System eine wichtige Rolle spielt.
In der Mehrzahl der Lebewesen spielt die RNA als Informationsträger eine der DNA untergeordnete Rolle: Die DNA ist hier das permanente Speichermedium für die genetische Information, die RNA dient als Zwischenspeicher. Nur RNA-Viren (die Mehrzahl aller Viren) nutzen RNA anstelle der DNA als permanentes Speichermedium. Zur Taxonomie von Viren unterscheidet man folgende RNA-Typen:
* dsRNA: Doppelstrang-RNA;
* ss(+)RNA: Einzelstrang-RNA, die als mRNA verwendet wird;
* ss(−)RNA: Einzelstrang-RNA, die als Matrize zur mRNA-Produktion dient.
Darüber hinaus nutzen einige Viren RNA als Replikationsintermediat (z. B. Retroviren und Hepadnaviren).
Abbau von RNA
Da ständig neue RNA gebildet wird und da zu unterschiedlichen Zeitpunkten verschiedene Transkripte benötigt werden (differentielle Genexpression), darf die RNA in der Zelle nicht zu stabil sein, sondern muss auch einem Abbau unterliegen. Dies geschieht mit Hilfe von RNasen, Enzymen, die die Verbindungen des Zucker-Gerüstes der RNA trennen und somit die Monomere (bzw. Oligomere) bilden, welche wieder zur Bildung neuer RNA verwendet werden können. Wann eine RNA abgebaut werden soll, wird dabei vor allem (aber nicht ausschließlich) durch die Länge des Poly-A-Schwanzes bestimmt, der mit zunehmender Verweildauer der RNA im Cytoplasma sukzessive verkürzt wird. Sinkt die Länge dieses Schwanzes unter einen kritischen Wert wird die RNA schnell degradiert. Zusätzlich können die RNAs stabilisierende oder destabilisierende Elemente enthalten, die eine weitere Regulation ermöglichen.
Zumindest bei der mRNA von Eukaryoten findet der RNA-Abbau nicht irgendwo im Cytoplasma statt, sondern in den so genannten „P-Bodies“ (processing bodies), die sehr reich an RNasen und anderen, am RNA-turnover (-Abbau)-beteiligten Enzymen sind. Zusammen mit Stress Granules dienen diese Körper weiterhin der kurzzeitigen Lagerung von mRNA und demonstrieren so wiederum die enge Verknüpfung des RNA-Metabolismus (hier Translation und RNA-Abbau).
Die RNA-Welt-Hypothese
Die RNA-Welt-Hypothese besagt, dass RNA-Moleküle bei der chemischen Evolution vermutlich Vorläufer der Organismen waren. Die Hypothese lässt sich ableiten aus der Fähigkeit der RNA zur Speicherung, Übertragung und Vervielfältigung genetischer Informationen sowie aus ihrer Fähigkeit, als Ribozyme Reaktionen zu katalysieren. In einer Evolutionsumgebung würden diejenigen RNA-Moleküle gehäuft vorkommen, die sich selbst bevorzugt vermehren.